W dzisiejszy artykuł będzie wprowadzeniem do procesów sorpcyjnych.
Ponadto odpowiemy na pytania, co to są procesy sorpcyjne, jak je dzielimy i czym się od siebie różnią.
Co kryje się pod pojęciem sorpcja?
Sorpcję najogólniej można przedstawić jako pochłanianie jednej substancji przez inną. Przykładem procesów sorpcyjnych z życia codziennego może być pochłanianie toksycznych substancji obecnych w organizmie przez węgiel aktywny.
Wyróżniamy dwa rodzaje procesów sorpcyjnych: absorpcję oraz adsorpcję.
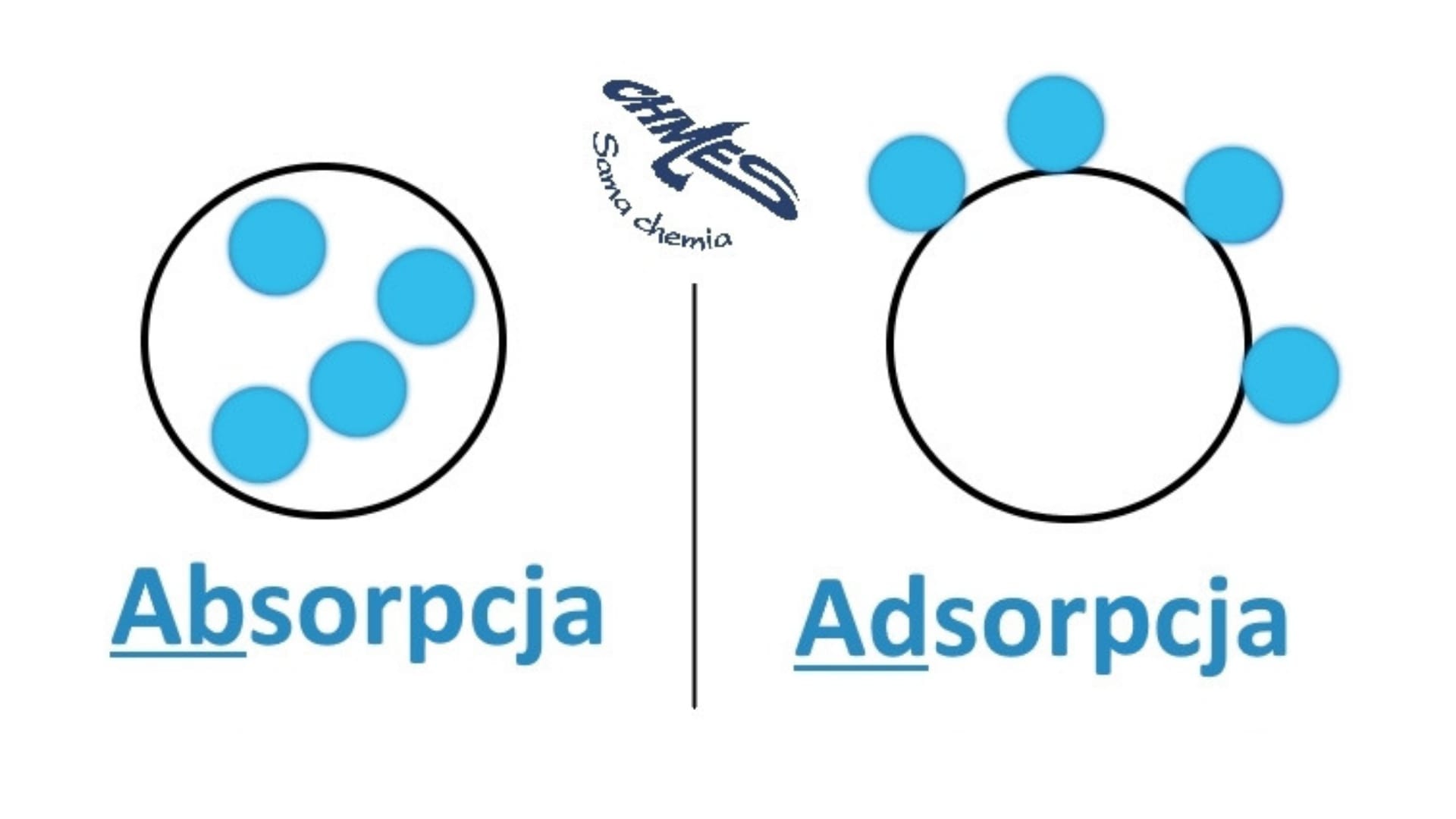
Absorpcja i Adsorpcja:
Absorpcja to proces polegający na pochłanianiu danej substancji przez całą objętość innej substancji (absorbenta).
Adsorpcja to proces polegający na pochłanianiu danej substancji jedynie na powierzchni adsorbenta.
Adsorpcja występuje więc na granicy dwóch faz, absorpcja w całej objętości fazy. Przykładem absorpcji jest pochłanianie zanieczyszczeń gazowych przez ciecz (w całej jej objętości).
Przykłady adsorpcji to wspominane wyżej pochłanianie toksyn przez węgiel aktywny, lub pochłanianie zapachów przez filtr węglowy w lodówce. Wreszcie, procesem odwrotnym do adsorpcji i absorpcji (czyli sorpcji) jest desorpcja.
W naszych artykułach skupimy się głównie na procesach adsorpcji oraz adsorbentach.
Na powierzchni adsorbentu działają różne siły, w zależności od ich rodzaju możemy wyróżnić adsorpcję chemiczną i fizyczną.
Adsorpcja fizyczna:
Adsorpcję fizyczną nazywamy także fizysorpcją, ponieważ zachodzi głównie pod wpływem sił oddziaływania międzycząsteczkowego (sił Van der Waalsa) oraz sił mostka wodorowego, dzięki czemu cała powierzchnia adsorbentu może być pokryta wieloma warstwami adsorbatu (czyli substancji pochłanianej). Wielkość fizysorpcji zależy od temperatury, ciśnienia lub stężenia adsorbatu. Ze względu na to, że proces adsorpcji jest egzotermiczny, podwyższenie temperatury lub obniżenie ciśnienia prowadzi do łatwej i szybkiej desorpcji. Liczba cząsteczek, która może być zaadsorbowana na powierzchni adsorbentu jest ograniczona i maleje ze wzrostem temperatury. Warunki sprzyjające adsorpcji to duża powierzchnia właściwa adsorbentu i niska temperatura.
Adsorpcja chemiczna:
Adsorpcja chemiczna (chemisorpcja) polega na wiązaniu się cząsteczki adsorbatu z powierzchnią za pomocą połączeń chemicznych (najczęściej kowalencyjnych). Jest ona często procesem nieodwracalnym, a zaadsorbowana substancja może być zdesorbowana tylko w postaci związku chemicznego lub usunięta jak substancja stała. Stopień pokrycia powierzchni adsorbentu jest niewielki – cząsteczki wiązane są tylko w miejscach aktywnych, między adsorbentem a adsorbatem tworzą się silne wiązania chemiczne, ciepło adsorpcji chemicznej jest więc dużo większe niż adsorpcji fizycznej. Obniżenie ciśnienia lub podwyższenie temperatury nie spowoduje desorpcji.